|
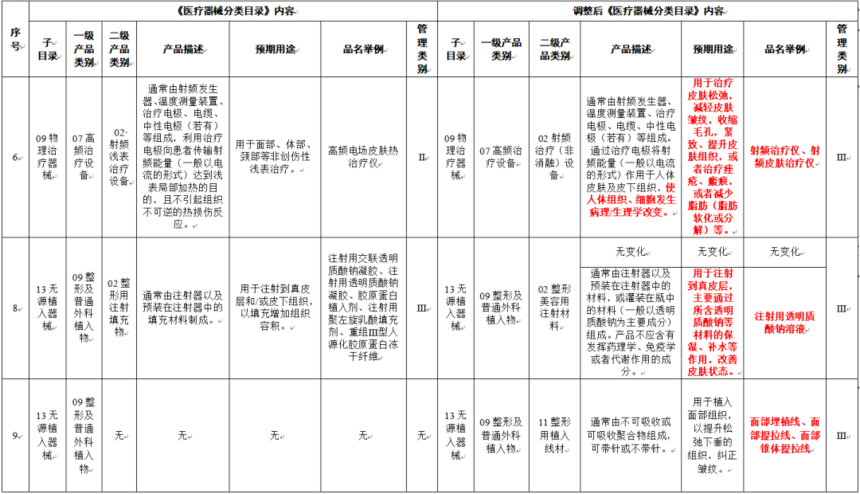
【政策解读】新规看2022年医美行业监管重点 水光针等被正式纳入三类医疗器械监管近日,国家药监局发布了《医疗器械分类目录》调整公告,明确表示“水光针类、射频仪器、埋植线”等产品正式纳入III类医疗器械管理范畴。
此次调整,涉及到的医美医疗器械有“水光针”、射频治疗(非消融)设备,以及“整形用植入线材”: 1、“水光针”调整为III类医疗器械 水光针是一种“中胚层疗法”,注射部位多为真皮层浅层至中层,具有补水、保湿效果。从成分看,狭义上,水光针仅指纯HA制剂的基础水光;广义上或实际应用中,可分为四大类,包括纯HA制剂、富含多种营养素的HA制剂、以某一其他成分为主的制剂和协同多个成分的配方制剂。 《目录》在整形美容注射材料里增加了一项产品描述:“用于注射到真皮层,主要通过所含透明质酸钠等材料的保湿、补水等作用,改善皮肤状态。”对应“水光针”类产品,被正式纳入III类医疗器械管理。 2、射频治疗(非消融)设备的管理类别,从 II 类提升至 Ⅲ 类,并对预期用途进行了细化 新《目录》已经明确,自2022年3月30日起,射频治疗(非消融)设备中射频治疗仪、射频皮肤治疗仪类产品按《医疗器械注册与备案管理办法》(国家市场监督管理总局令第47号)的规定申请注册。相关注册人、生产企业应当主动向所在地省级药品监督管理部门报告产品按医疗器械研制注册计划等。 自2024年4月1日起,射频治疗仪、射频皮肤治疗仪类产品未依法取得医疗器械注册证不得生产、进口和销售。 3、新增“整形用植入线材”,将“面部埋植线、面部提拉线、面部锥体提拉线”等埋线类产品纳入III类医疗器械管理。 二、政策解读 此次《目录》中提及到的医美器械产品,均为当下爆火的轻医美品类,政策监管的收紧或将对轻医美赛道产生巨大影响。同时,此前不需要医疗器械类别管理、或者需要按照II类医疗器械管理的,都要重新进行审批,上市之路将面临新挑战。 我国对于医疗器械有着严格的分类标准,III类医疗器械属于最高级别的医疗器械,也是必须严格控制的医疗器械。III类医疗器械是指植入人体,用于支持、维持生命,对人体具有潜在危险,对其安全性、有效性必须严格控制的医疗器械。 1、鱼龙混杂的水光针将趋于正规 水光针作为热门轻医美产品风靡近十年,其简单有效、价格便宜、创伤小等优势,深受消费者青睐,有数据表示,预计2025年水光针市场规模将在200亿元以上。 此监管条例一出,市面上所称的“水光针”将正式纳入III类医疗器械管理,水光针市场当下快速的增长趋势或将受限;与此同时,市场上的假货、水货等针剂乱象问题也将得到改善。 2、爆火的家用“射频美容仪”或将成为过去时 在“颜值经济”的催生下,抗衰紧致类射频美容仪正成为年轻消费者“新宠”,家用射频美容仪、功率较大的射频院用美容仪市场规模不断扩大,成为近几年家庭美容领域的一大风口。 一直以来,在医美行业内都存在“射频治疗仪器到底是医疗器械还是家用电器”的争议。此次《医疗器械分类目录》将射频类美容仪器明确规定为III类医疗器械,其中不光是美容机构所使用的大型射频美容仪器,当前爆火的家用射频美容仪也都纳入了医疗器械监管范畴。 此外,争议较多的热玛吉五代,比对《医疗器械分类目录》(2022年第30号)规定,作为射频治疗仪的热玛吉,也毫无疑问地应当按照第三类医疗器械进行申报管理。 此次《医疗器械分类目录》调整,是近年来国家对医美行业监管不断收紧的再一次重拳出击,执法监督范畴也从地域性扩大为全国性,力度不断加强。加上近年来多项强监管措施,这都预示着国家对于医疗器械的管理更加规范严格,医疗美容行业也将走向越来越合规化发展之路。 湖南省美容美发化妆品行业协会今后将继续履行职责和义务,发挥行业协会作用,积极配合政府相关部门工作,宣传贯彻政府有关政策,对行业产品、服务质量、经营情况等进行严格监督,营造安全消费环境,为湖南美业高质量可持续发展贡献力量。
|